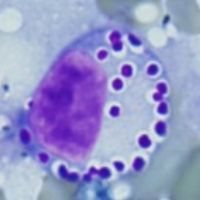
犬の組織球性肉腫の分子病態の解明と新規治療法の開発
犬の腫瘍性疾患の中でも組織球性肉腫は極めて予後不良な疾患です。我々はこの疾患の約40%でTP53遺伝子に変異が認められることを報告しました(Asada et al., J. Vet. Med. Sci. 2017)。またこれらの遺伝子変異がTP53遺伝子の機能に与える影響に関する検討(Asada et al., Am. J. Vet. Res. 2019)やこれら変異が腫瘍組織内で不均一に認められること(Asada et al., J. Vet. Med. Sci. 2019)、さらにはその臨床的意義(Asada et al., Res. Vet. Sci. 2019)も報告しています。
さらに現在は次世代シーケンサーを用いたゲノムDNA配列やトランスクリプトーム解析によってその分子病態を網羅的に解析することで、様々な細胞内シグナル経路における異常を見出しました(Asada et al., Sci. Rep. 2023)。現在はこれらの知見をもとに、組織球性肉腫に対して効果を示す可能性がある新たな抗がん剤(分子標的薬)を検討しています。
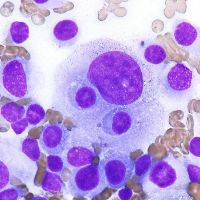
犬のリンパ腫におけるエクソソームが果たす役割の検討
リンパ腫は動物においてもっとも多く認められる造血器腫瘍ですがその分子病態は未だ不明な点が多いのが現状です。
近年、腫瘍性疾患の進行には腫瘍細胞自体の異常だけではなくその周囲の微小環境とのコミュニケーションが非常に重要な役割を果たしていることが明らかとなってきました。我々はその細胞間のコミュニケーションに用いられる様々な因子の中でも特に細胞外小胞であるエクソソームに着目し、犬のリンパ腫細胞由来のエクソソームが内包する分子プロファイルを明らかにしました(Asada et al., PLoS One 2019)。
この研究成果を元に、腫瘍細胞由来のエクソソームが末梢血由来単球および活性化T細胞のそれぞれの遺伝子発現プロファイルや機能にどのような変化をもたらすかも検討しその詳細を明らかにしました(Tani et al., J Vet Med Sci 2022, Weng et al., Cancer Cell Int, 2023)。
将来的にはこれらの研究から明らかとなる新規分子病態を基にした新規治療法の開発を目指しています。
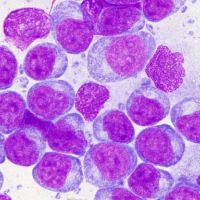
犬のリンパ腫における化学療法耐性機構の解明
リンパ腫症例のほとんどは、当初は化学療法に非常によく反応することが知られています。しかしながら治癒は非常に困難であり、いずれ化学療法に対する耐性を獲得してしまうことが治療のもっとも大きな壁となっています。
この壁を越えるべく、我々はこれまでに化学療法耐性をもたらす分子機構の解明を目指し、精力的に研究を行ってきました(Tomiyasu et al., Vet. Sci. 2015 Review)。しかしながらこれらの研究成果から既知の因子では犬のリンパ腫における化学療法耐性は説明できないことが明らかとなったため網羅的な遺伝子発現プロファイルの解析を行ったところ、近年我々は新規耐性関連分子を明らかとすることに成功しました(Suenaga et al., Vet. J. 2017, Hsu et al., PLoS One, 2021, Tani et al., Res Vet Sci, 2021)。
また、我々は初期寛解導入化学療法後の転機(長期寛解あるいは早期再発)を規定する分子プロファイルを同定することにも成功しました(Toyoda et al., J Vet Med Sci, 2024)。
これらの知見から、特に腫瘍細胞と腫瘍微小環境中の免疫細胞との相互作用に着目しながら、臨床例において化学療法耐性をもたらす詳細な分子機構の解析を行っています。
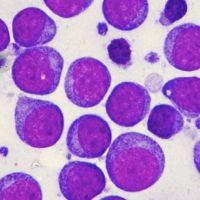
猫のリンパ系腫瘍における分子病態の解明
猫においてもリンパ系腫瘍はもっとも多い造血器腫瘍であり、犬と同様に当初は化学療法に非常によく反応することが知られていますがやはり完治が困難な疾患です。
我々はこれまでにいくつかの猫のリンパ系腫瘍の臨床的特徴に関して明らかにしてきました(Tomiyasu et al., J Small Anim Pract, 2018, Nakazawa et al., J Vet Med Sci, 2021)。
一方で、猫のリンパ系腫瘍が持つ分子病態に関してはまだまだ未解明な点が多いのが現状です。そこで我々は現在、網羅的な遺伝子発現解析を用いて分子異常の探索を開始しています。